Un aneurisma è la dilatazione di un tratto di arteria superiore al 50% del diametro, con perdita del parallelismo tra le pareti dell'arteria stessa.
L'aorta è l'arteria più grande del corpo umano e si estende dal cuore alla quinta vertebra lombare. Decorre nel torace, quindi passa in addome attraversando il diaframma.
Il tratto di aorta al di sotto del diaframma costituisce l'aorta addominale, ed ha un calibro di circa 2-2,5 cm. 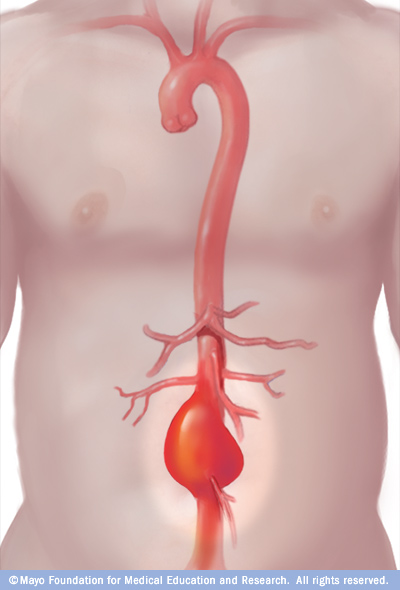
Gli aneurismi dell'aorta addominale (AAA) sono relativamente comuni e potenzialmente mortali.
Soggetti a maggior rischio per l'aneurisma dell'aorta addominale sono i maschi oltre i 65 anni che sono portatori di arteriopatia periferica aterosclerotica.
In anamnesi si rilevano con grande frequenza tabagismo, malattia ostruttiva polmonare cronica e ipertensione. Cause meno frequenti sono la sindrome di Marfan e la sindrome di Ehlers-Danlos, collagenopatie vascolari e aneurismi micotici.
I soggetti che hanno un parente di primo grado con aneurisma dell'aorta addominale hanno un rischio più elevato.
Gli AAA sono solitamente asintomatici fino al momento in cui si espandono o si rompono.
La maggior parte degli AAA sono palpabili al normale esame fisico. Talvolta sono proprio i pazienti a riferire una pulsazione addominale anomala.
La presenza di una massa addominale pulsante ed espansibile è virtualmente diagnostica, ma viene riscontrata in meno della metà dei casi. Le difficoltà sono ancora maggiori nei soggetti obesi.
La palpazione dell'addome, in pazienti in cui si sospetta la presenza di AAA, può essere eseguita senza particolari timori, perché non c'è evidenza che la rottura dell'aneurisma possa essere provocata da questa manovra. L'aneurisma può essere palpato nell'addome superiore sulla linea mediana o leggermente verso sinistra: la biforcazione aortica, infatti, si proietta in corrispondenza dell'ombelico.
L'esame fisico deve essere completato con la palpazione dei polsi periferici, per determinare la presenza di arteriopatia obliterante periferica o di aneurismi dell'arteria poplitea (25-50% dei casi). È importante anche determinare la presenza di stenosi o occlusione delle arterie carotidi e succlavie.
Talvolta l'aneurisma dell'aorta addominale può provocare sintomi da compressione locale: senso di sazietà precoce, nausea, vomito, coliche renali per compressione degli ureteri, trombosi venosa iliacofemorale per compressione diretta delle vene.
Il dolore lombare può essere provocato dall'erosione dell'AAA a carico dei corpi delle vertebre adiacenti.
Altri sintomi comprendono dolori addominali vaghi, dolore inguinale, fenomeni embolici a carico delle dita dei piedi (p. es. livedo reticularis, o gangrene ischemiche parcellari) e febbre.
In rari casi piccoli aneurismi dell'aorta addominale possono andare incontro a trombosi acuta, provocando improvvisa claudicatio intermittens o una vera e propria sindrome da barrage aortico acuto (ischemia acuta dell'emisoma inferiore).
È importante distinguere se vi è una progressione nei sintomi, perché ciò potrebbe indicare la possibilità di espansione con rischio di rottura imminente.
Un AAA in fase di espansione provoca un dolore improvviso, grave e costante in regione lombare, al fianco, all'addome, o all'inguine.
L'esordio può avvenire anche con una sincope: in questo caso il dolore è meno apprezzabile.
I pazienti possono avvertire dolore non particolarmente grave per relativamente molto tempo prima della rottura.
Il dolore all'inguine è piuttosto insidioso quando si presenta come unico sintomo d'esordio: questo avviene quando l'espansione retroperitoneale provoca pressione su uno dei due nervi femorali che decorrono sui muscoli psoas in vicinanza dei grossi vasi addominali. Questo sintomo può presentarsi isolatamente e rappresenta una vera e propria trappola diagnostica.
Anche se la rottura di un aneurisma dell'aorta addominale può presentarsi con modalità variabili, la manifestazione più tipica della rottura è un violento dolore addominale o lombare associato a tachicardia e ipotensione, in presenza di una massa addominale pulsante ed espansibile (30-50% dei casi).
La diagnosi può essere confusa con una colica renale, una diverticolite, un'ernia incarcerata, un dolore legato a patologia della colonna lombare.
Un episodio di ipotensione transitoria dovrebbe richiamare l'attenzione sulla possibilità della rottura di un AAA, soprattutto se accompagnato da perdita di coscienza temporanea: questo sintomo può progredire fino ad uno shock ipovolemico nel giro di poche ore.
L'esordio della rottura di un AAA può avvenire direttamente con un dolore improvviso accompagnato da shock ipovolemico: i segni sono la cianosi, le marezzature, l'alterazione dello stato mentale, la tachicardia e l'ipotensione.
Mentre l'improvvisa insorgenza di dolore dovuto alla rottura di un AAA può essere piuttosto drammatica, i segni fisici associati possono essere insidiosi e di difficile riscontro. I pazienti possono manifestare normali segni vitali in presenza di un AAA rotto, come conseguenza del tamponamento dell'ematoma esercitato dal retroperitoneo.
Almeno il 65% dei pazienti con un AAA rotto muore per collasso cardiovascolare acuto prima di giungere in ospedale.
Un AAA può rompersi nella vena cava inferiore o nelle vene iliache, dando luogo ad ampie fistole arterovenose. L'ampia portata di queste fistole produce effetti emodinamici improvvisi e pericolosi, perché può portare rapidamente all'insufficienza cardiaca congestizia. Altri sintomi delle fistole aorto-cavali sono: tachicardia, edema degli arti inferiori, insufficienza renale acuta, ischemia periferica, fremito (thrill) addominale, soffio vascolare addominale.
Infine, un AAA può rompersi nella quarta porzione del duodeno. In questi casi, i pazienti possono presentare un sanguinamento gastrointestinale intermittente (sanguinamento sentinella o herald bleeding), che termina con un'emorragia gastrointestinale irrefrenabile.
Studi sviluppati negli ultimi due decenni hanno dimostrato che l'AAA può essere efficacemente diagnosticato e descritto attraverso un'ecografia dell'addome, esame che spesso viene eseguito per altre motivazioni e che rivela la presenza di questa malattia in modo inaspettato.
Attraverso l'ecografia si possono ricavare pressoché tutti i parametri utili alla diagnosi: diametri anteroposteriore e trasverso, lunghezza, decorso, presenza di trombo endoluminale, stato del colletto e delle arterie renali.
Anche in caso di rottura dell'AAA, l'ecografia permette di ottenere in pochi secondi la certezza della diagnosi.
La facilità di esecuzione e l'innocuità dell'esame permettono di eseguire anche programmi di screening nella popolazione più a rischio e di monitorare in modo non invasivo il tasso di crescita dell'AAA.
La TAC con mezzo di contrasto è l'esame di scelta per definire con maggior precisione tutti gli aspetti morfologici che consentono di programmare l'intervento chirurgico, compreso lo stato delle arterie iliache e femorali e delle arterie viscerali.
Attraverso questo esame è possibile ottenere alcune delle informazioni indispensabili per stabilire quale tecnica chirurgica è più conveniente per quel determinato paziente, anche attraverso ricostruzioni 3D e simulazioni. 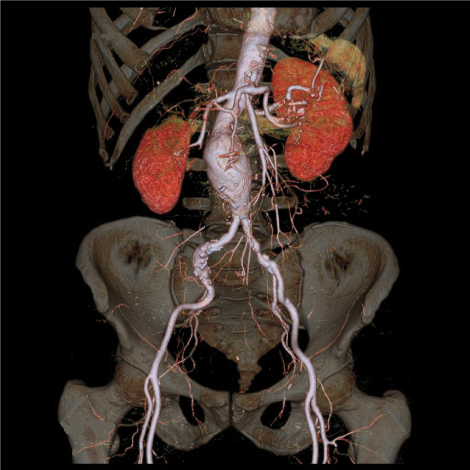
La Tac con mezzo di contrasto viene anche utilizzata per il follow-up dei trattamenti endovascolari, per la precisione nell'individuare le perdite delle endoprotesi e i rifornimenti residui della sacca aneurismatica (endoleaks), che richiedono procedure aggiuntive.
La risonanza magnetica nucleare consente di ottenere le stesse indicazioni della TAC, che, però, rimane attualmente la tecnica diagnostica preferita per la programmazione dell'intervento.
Il trattamento dell'AAA è chirurgico anche per i soggetti che non hanno sintomi, perché i trattamenti farmacologici e medici, nel tempo, hanno una mortalità del 100% per rottura.
La decisione di trattare un aneurisma in elezione tiene conto del rischio operatorio, del rischio di rottura e dell'attesa di vita del paziente.
Quando i diametri dell'aneurisma superano i 5,5 cm il rischio di rottura aumenta in modo esponenziale.
| Diametro dell'AAA e rischio stimato di rottura per anno |
| DIAMETRO (cm) |
RISCHIO DI ROTTURA (%/anno) |
| < 4 |
0 |
| 4 - 5 |
0.5 - 5 |
| 5 - 6 |
3 - 15 |
| 6 - 7 |
10 - 20 |
| 7 - 8 |
20 - 40 |
| > 8 |
30 - 50 |
Pertanto, l'indicazione alla chirurgia viene considerata quando si raggiunge questo limite dimensionale, anche perché tutti gli studi hanno dimostrato che al di sotto di questa soglia il trattamento chirurgico non migliora la sopravvivenza. La soglia pare più bassa (4,5 cm) nel sesso femminile.
L'intervento è giustificato per piccoli aneurismi (4-5 cm) in pazienti giovani e in buone condizioni generali.
Anche un tasso di crescita annuo superiore a 1 cm deve essere considerato motivo per indicare l'intervento chirurgico perché aumenta il rischio di rottura.
Altre condizioni influenzano il rischio di rottura di un AAA: tabagismo, storia familiare, ipertensione arteriosa, caratteristiche dell'aneurisma, tensione della parete.
| Fattori che influenzano il rischio di rottura di un AAA |
| |
RISCHIO BASSO |
RISCHIO INTERMEDIO |
RISCHIO ELEVATO |
| Diametro |
< 5 cm |
5 - 6 cm |
> 6 cm |
| Tasso di espansione |
< 0.3 cm/anno |
0.3 - 0.6 cm/anno |
> 0.6 cm/anno |
| Fumo / BPCO |
nessuno o lieve |
moderato |
grave / uso di steroidi |
| Storia familiare |
Nessun congiunto |
Un parente |
Più di un parente |
| Ipertensione arteriosa |
Pressione normale senza terapia |
Ipertensione controllata dalla terapia |
Ipertensione con controllo farmacologico difficile |
| Forma dell'AAA |
Fusiforme |
Sacculare |
Molto eccentrico |
| Tensione di parete |
Bassa (<35 N/cm2) |
Media (40 N/ cm2) |
Elevata (>45 N/ cm2) |
| Sesso |
|
Maschio |
Femmina |
| BPCO: Broncopneumopatia cronica ostruttiva |
Nella valutazione deve essere tenuto presente soprattutto il rischio operatorio del singolo paziente, che è determinato dalla comorbilità: tra le condizioni più rilevanti, l'età, il sesso, la funzionalità renale, la performance cardiopolmonare.
| Rischio operatorio per aneurismectomia laparotomica (open repair) |
| BASSO |
INTERMEDIO |
ELEVATO |
| Età < 70 anni |
Età 70 - 80 anni |
Età > 80 anni |
| Fisicamente attivo |
Moderatamente attivo |
Inattivo o debilitato |
| Nessuna patologia cardiaca conclamata |
Miocardiopatia coronarica stabile; Storia di infarto del miocardio; Frazione di eiezione del ventricolo sinistro <35% |
Malattia coronarica importante; Angina instabile; Infarto del miocardio recente; Insufficienza cardiaca; Frazione di eiezione del ventricolo sinistro <25% |
| Nessuna malattia concomitante importante |
Broncopneumopatia cronica ostruttiva moderata |
Broncopneumopatia cronica ostruttiva grave; dispnea a riposo; dipendenza dall'ossigeno |
| Creatininemia <2.0 mg/dL |
Creatininemia 2.0 - 3.0 mg/dL |
Creatininemia > 3.0 mg/dL |
| Anatomia normale |
Caratteristiche anatomiche difficili |
Caratteristiche particolari dell'aneurisma |
| |
|
Insufficienza epatica (albuminemia <2 g/dL; allungamento del PT) |
Mortalità operatoria attesa:
1% - 3% |
Mortalità operatoria attesa:
3% - 7% |
Mortalità operatoria attesa:
5% - 10%
ciascuna condizione aumenta il rischio operatorio dal 3% al 5% |
Va da sé che anche l'esperienza del chirurgo e il livello di attrezzature, servizi ed organizzazione dell'ospedale giocano un ruolo determinante.
Come si vede, la decisione se operare o meno un AAA è molto complessa e deve tenere conto della combinazione di molti fattori che contribuiscono sia al rischio di rottura, sia al rischio operatorio.
Possiamo quindi ritenere ancora meritevole di considerazione l'affermazione del medico Antillo, vissuto nel III sec. dC, secondo cui "rinunciare al trattamento di qualsiasi aneurisma è folle, ma è ugualmente pericoloso operarli tutti".
La chirurgia in elezione può essere effettuata in due modi: per via laparotomica (open repair: OR) o per via endovascolare (endovascular aneurysmal repair: EVAR).
La scelta della tecnica dipende sia dalle preferenze del chirurgo, sia dall'esistenza di caratteristiche geometriche delle arterie e dell'aneurisma che consentono l'accesso endovascolare.
Il paziente è in anestesia generale. Si utilizza un dispositivo per il recupero del sangue.
L'aorta è raggiunta per via anteriore transperitoneale, con eviscerazione del piccolo intestino.
Il flusso di sangue viene interrotto nell'aorta al di sotto delle arterie renali e nelle arterie iliache con delle pinze non traumatiche (clamp). 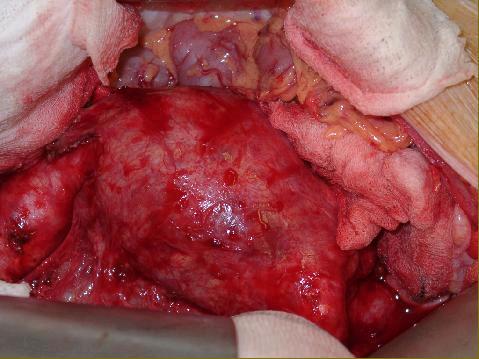
L'aneurisma viene aperto e svuotato del suo contenuto: in questa fase si provvede a suturare le arterie lombari che sboccano a coppie sulla parete posteriore dell'aorta. Anche l'arteria mesenterica inferiore viene suturata. L'aorta malata viene quindi sostituita con una protesi tubulare sintetica. Se necessario, si sceglie una protesi biforcata (a calzoncino) quando anche le arterie iliache sono compromesse. 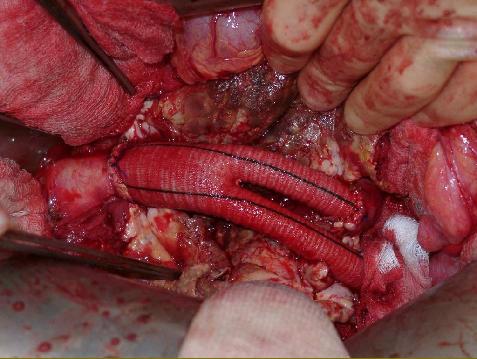
Le branche della protesi biforcata possono anche essere portate direttamente sulle arterie femorali, alla radice della coscia, se necessario. Raramente è richiesto il reimpianto dell'arteria mesenterica inferiore sulla protesi.
L'intervento termina con la copertura della protesi con la parete dell'aneurisma, ormai "vuoto", e con la ricostruzione delle strutture attraversate per raggiungere l'aorta.
La presenza di una protesi richiede la profilassi antibiotica, per ridurre il rischio di infezione.
L'arresto del flusso di sangue alle gambe richiede l'uso di anticoagulanti (eparina) o per via generale o anche solo localmente.
Per poter effettuare questo intervento, l'aorta al di sotto delle arterie renali deve avere un tratto sano (colletto) di circa 1,2 centimetri e le arterie iliache e femorali devono avere un diametro sufficiente al passaggio degli strumenti. Anche angolature troppo strette delle arterie possono costituire ostacoli alla buona riuscita dell'intervento.
L'intervento è eseguito preferibilmente in anestesia generale, ma può essere utilizzata anche una anestesia spinale alta, in casi adatti.
E' necessaria una anticoagulazione con eparina per via endovenosa.
Attraverso due incisioni agli inguini si preparano le arterie femorali. Attraverso queste si introducono guide e cateteri per il controllo angiografico intraoperatorio.
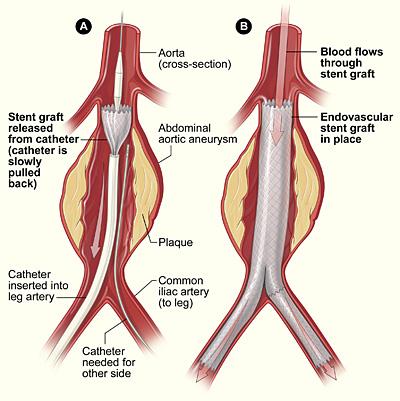
Lungo la guida posta all'interno dell'arteria femorale di un lato, si introduce il dispositivo di rilascio dello stent (gabbia metallica) rivestito al suo interno di materiale impermeabile (Dacron o PTFE), se ne controlla la posizione e si rilascia la protesi, che viene fatta aderire al colletto dilatandola con un palloncino.
La protesi è fatta come un calzoncino con una delle due gambe (branche) molto corta. La branca più lunga viene fatta aderire all'arteria iliaca attraversata dal dispositivo di rilascio.
Attraverso l'arteria femorale del lato opposto, si introduce una guida dentro la branca corta della protesi, quindi lungo la guida si introduce il secondo dispositivo di rilascio, che consente di dare la giusta lunghezza alla branca aggiungendo un secondo stent rivestito, questa volta tubulare. Anche da questo lato, l'adesione delle due protesi tra loro e con l'arteria nativa viene perfezionata con un palloncino.
Infine, si controlla con un'angiografia il buon funzionamento dell'impianto e l'esclusione della sacca dell'aneurisma da qualsiasi rifornimento di sangue. L'intervento termina con la rimozione degli strumenti e la riparazione delle arterie femorali.
Un aneurisma in rottura deve essere operato al più presto possibile, perché la mortalità aumenta se il paziente si presenta in shock. La mortalità in urgenza è attorno al 50% di coloro che giungono in sala operatoria.
Secondo uno studio multicentrico randomizzato su 613 pazienti con diagnosi di AAA rotto, pubblicato nel 2014, non si hanno differenze tra la mortalità degli AAA in rottura operati per via laparotomica e quelli operati con EVAR (37,4% e 35,4%), anche se le donne hanno un migliore risultato dall'EVAR rispetto agli uomini.
Anche i costi sono risultati simili, mentre la degenza è risultata più breve per i pazienti trattati con EVAR.
Va notato, tuttavia, che la selezione dei pazienti, rispetto al tipo di intervento, ha tenuto conto delle caratteristiche geometriche dell'aorta e delle arterie iliacofemorali, avviando i casi più compromessi all'intervento laparotomico.
È molto importante anche l'assistenza anestesiologica e rianimatoria dopo l'intervento in urgenza.
Riferimenti:
http://www.mayoclinic.org/diseases-conditions/abdominal-aortic-aneurysm/basics/definition/con-20023784
http://emedicine.medscape.com/article/1979501-overview
http://www.nhs.uk/conditions/Repairofabdominalaneurysm/Pages/Introduction.aspx
http://www.ncbi.nlm.nih.gov/pubmedhealth/PMH0062939/